16 Septembre 1975 : le
CHU Côte
de Nacre accueille son premier malade.
1976 : un total de 4481
personnes,
chirurgiens, médecins, infirmières, soignants et
soignantes, techniques et administratifs est dénombré.
1978 : le Centre
Esquirol, abritant la
psychiatrie, ouvre ses portes.
1980 : ouvertures du
nouveau service de
gynécologie-obstétrique, de 2 pavillons au Centre pour
Personnes Agées et des nouveaux
pavillons de néphrologie.
figure3
: bâtiment
IRM [14]
1990
: création
d'une
unité IRM.
1994 : ouverture d'une
seconde IRM.
1998
: acquisition d’un
gamma caméra "double tête" dans le service de biophysique
médicale. Restructuration du service de rhumatologie (Côte
de Nacre).
5 Décembre 2005 :
ouverture du
bâtiment polyvalent à l'hôpital Clemenceau
accueillant les services de pédiatrie et de
pédopsychiatrie.
L’avenir
du CHU de Caen est basé sur un plan directeur. En effet,
celui-ci a pour but la création de 8 pôles
médico-chirurgicaux et de 4 ensembles d’activités. Cela a
pour objectif de regrouper les disciplines afin d’optimiser les
performances du CHU. L’hôpital Côte de Nacre sera le site
où le regroupement s’effectuera.
Dans
les
années à venir, l’un des premiers regroupements à
s’effectuer sera celui du pôle mère-enfant.
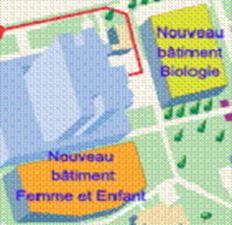
Figure4 :
Projet d’implantation
de nouveaux bâtiments [15]
Aujourd’hui,
cette
activité est en partie sur le site de Clemenceau mais devra donc
rejoindre le site de Côte de Nacre. Ce pôle
mère-enfant comprendra la Pédiatrie médicale, la
Chirurgie Pédiatrique, la Néonatalogie, la
Gynécologie Obstétrique. Pour la construction de ce
pôle mère-enfant, le CHU de Caen met en place un projet
PPP (Partenariat Public Privé). Ce projet est le premier sur le
plan national au niveau des structures hospitalières. En effet,
le CHU de Caen a décidé de confier à un
opérateur privé la conception, la réalisation,
l’entretien et le financement de cette nouvelle infrastructure. Le CHU
sera alors locataire de ces bâtiments. Une réflexion est
en cours pour la création d'un pôle Biologie. [2]
1.2
Sites du CHU
Le
CHU de Caen répartit ses lits et ses plateaux techniques sur 3
sites implantés sur la commune de Caen : l'hôpital
Côte de Nacre, l'hôpital Clemenceau et le Centre pour
Personnes Agées. Visite détaillée de chacun de ces
lieux.
Hôpital
Côte de Nacre :
mis en
service en 1975, dans une structure monobloc, comprend 1137 lits. Son
activité est particulièrement orientée vers la
médecine et la chirurgie adultes. L'établissement
hospitalise annuellement plus de 57 000 patients dont 20 000 en
urgences. Pour assurer au mieux ses missions, il fera l'objet, dans les
années à venir d'importantes opérations de
restructuration conformément au Projet Médical et au
Projet d'Etablissement.
Figure5 : Hôpital Cote de Nacre [16]
|
|
figure5:hôpital
cote de
nacre [16]
Hôpital
Clémenceau :
structure
pavillonnaire traditionnelle de 390 lits, conçue à la fin
du 19ème siècle, est un site orienté
principalement autour du pôle mère-enfant. Il comporte
aussi des secteurs spécifiques : alcoologie, traitement de la
douleur et du sommeil. Près de 1206 professionnels sont
attachés à Clemenceau, et chaque année plus de 33
000 patients y sont soignés. Il est le symbole historique de
l'hospitalisation publique à Caen.
figure6:hôpital
Clémenceau [17]
Centre pour Personnes
Agées
(C.P.A.) :
établissement destiné à l'accueil des personnes
âgées dépendantes, dispose actuellement de 270 lits
répartis en Unités de Soins de Longue Durée
(U.S.L.D.), Soins de Suite et de Réadaptation (S.S.R.) et Maison
de Retraite. Les résidants sont pris en charge par 190 agents,
soignants et personnel des services logistiques (173,38 ETP). Le C.P.A.
vient de faire l'objet d'un programme de modernisation et de
restructuration de l'activité de soins. [3]
Figure6 : hôpital Clémenceau [1
|
|
Figure7 : Centre Personnes Agées [18]
|
|
figure7:Centre
Personnes
Agées [18]
1.3
Repartition de
l activite
Répartition
des lits et
places installés par discipline [4]
| CAPACITE (lits et places
installés) |
|
LITS |
PLACES |
| Médecine |
|
675
|
47
|
| Chirurgie |
|
474
|
18
|
| Obstétrique |
|
113
|
20
|
| Soins de suite et de
réadaptation |
|
27
|
0
|
Psychiatrie
(adultes et pédopsychiatrie) |
|
59
|
20
|
| Soins de Longue Durée -
Maison de
retraite |
|
253
|
0
|
| TOTAL |
|
1601
|
105
|
Figure 8 :
tableau des répartitions des lits [19]
Hôpital Côte de Nacre
:
Activités
cliniques :
- médecine :
- cardiologie,
- endocrinologie-diabétologie,
- hépato-gastro-entérologie
et nutrition,
- maladies infectieuses et tropicales,
- médecine
générale,
- médecine gériatrique,
- médecine interne,
- neurologie,
- onco-hématologie
pédiatrique,
- pneumologie,
- réanimation médicale
adulte et pédiatrique,
- rhumatologie.
- chirurgie :
- chirurgie digestive,
- chirurgie générale et
viscérale,
- chirurgie infantile,
- chirurgie maxillo-faciale et
plastique,
- chirurgie thoracique et
cardio-vasculaire,
- neurochirurgie,
- ophtalmologie,
- orthopédie - traumatologie,
- oto-rhino-laryngologie,
- réanimation chirurgicale
adulte et pédiatrique,
- urologie,
- chirurgie ambulatoire (clinique de
la Miséricorde),
- lithotritie (clinique St Martin),
- autres :
- médecine physique et
réadaptation,
- santé au travail et
pathologie professionnelle,
- SAMU/SMUR,
- urgences.
Activités
médico-techniques :
- anesthésie,
- blocs opératoires,
- imagerie :
- échographie,
- IRM,
- médecine nucléaire,
- neuroradiologie,
- radiologie générale,
- scanographie.
- laboratoires :
- anatomie pathologique,
- biochimie,
- explorations fonctionnelles,
- génétique et
reproduction (cytogénétique prénatale, CECOS et
Spermiologie),
- hématologie et centre de
traitement de l’hémophilie,
- microbiologie,
- pharmacologie - toxicologie,
- Radio-immunologie
1.4
Les equipements
Plateau
Technique du C.H.U. de Caen [5] :
Imagerie :
- 15 salles de radiologie
conventionnelle
- 2 salles de radiologie
numérisée
- 5 salles d’angiographie
numérisée
- 1 mammographie
- 18 échographes doppler
- 2 scanners
- 2 I.R.M
- 3 gamma-caméras
- 1 TEP-scan
figure
9 : scanner [20]
Laboratoires:
- Anatomie Pathologique
- Biochimie
- Biophysique
Médicale
- Département
Génétique et Reproduction (Cytogénétique
Prénatale, Spermiologie, CECOS)
- Electromyographie
- Explorations
Fonctionnelles
- Expl. °
Fonctionnelles Neurologiques
- Hématologie
- Hygiène
Hospitalière
- Immunologie
- Pharmacologie
- Microbiologie
- Toxicologie
- Virologie
figure
10 : laboratoire [21]
38
salles
d'opérations : réparties en 12 blocs
opératoires sur 6 étages.
Figure11:salle
d'opération [22]
1.5
Presentation du service
biomedical
Le
service
Biomédical, localisé sur le site de Côte de Nacre
au 22ème étage, a en charge la maintenance des
différents dispositifs médicaux ainsi que l’achat de
nouveaux équipements.
Le
service est
composé de 22 personnes :
- 5 ingénieurs (4 biomédicaux, 1
radioprotection),
- 15
techniciens biomédicaux,
- 1
personne assurant le support technique,
- 1
secrétaire.
Les
techniciens sont répartis majoritairement sur le site Côte
de Nacre mais également sur le site Clemenceau. Ils sont
organisés par équipe (binôme sauf pour les blocs de
CDN) avec différentes spécialités (Imagerie,
Laboratoire, Monitorage, Réanimation, Chirurgie,
Hémodialyse,…). Ils s’occupent notamment de la maintenance
corrective et préventive et du suivi des équipements sous
contrat.
Les
ingénieurs sont aussi spécilalisé par pôle
(anesthésie/réanimation, imagerie, laboratoire, bloc
opératoire, exploration fonctionelle, dialyse, endoscopie
etc...)
L’équipement
médical :
Les
dépenses relatives aux équipements médicaux
représentent 5 389 252 € en 2006 dont 1 711 495 relevant du plan
d'équipement médical :
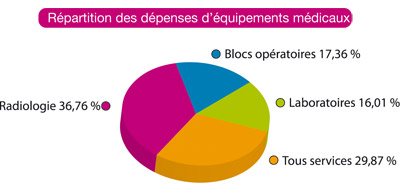
Figure 12 : répartition des
dépenses d'équipements médicaux [23]
Le CHU s’est acquitté en 2006 du
coût d’installation de la nouvelle IRM acquise pour un montant de
1 393 888 € expliquant le pourcentage de dépenses important sur
le secteur imagerie.
Le biomédical :
5 150
interventions de maintenance ont été
réalisées par le service biomédical sur
l’équipement médical du CHU (12000 équipements) .
Un tiers de ces interventions correspondent à des actions de
maintenance préventive et de contrôles de performance des
dispositifs médicaux.
Les
dépenses liées à la maintenance connaissent une
diminution de 9 % par rapport à 2005 et atteignent 2,44 M€ (dont
1,78 M€ pour les seuls contrats de maintenance). Actuellement le
taux de renouvellement est de 75%.
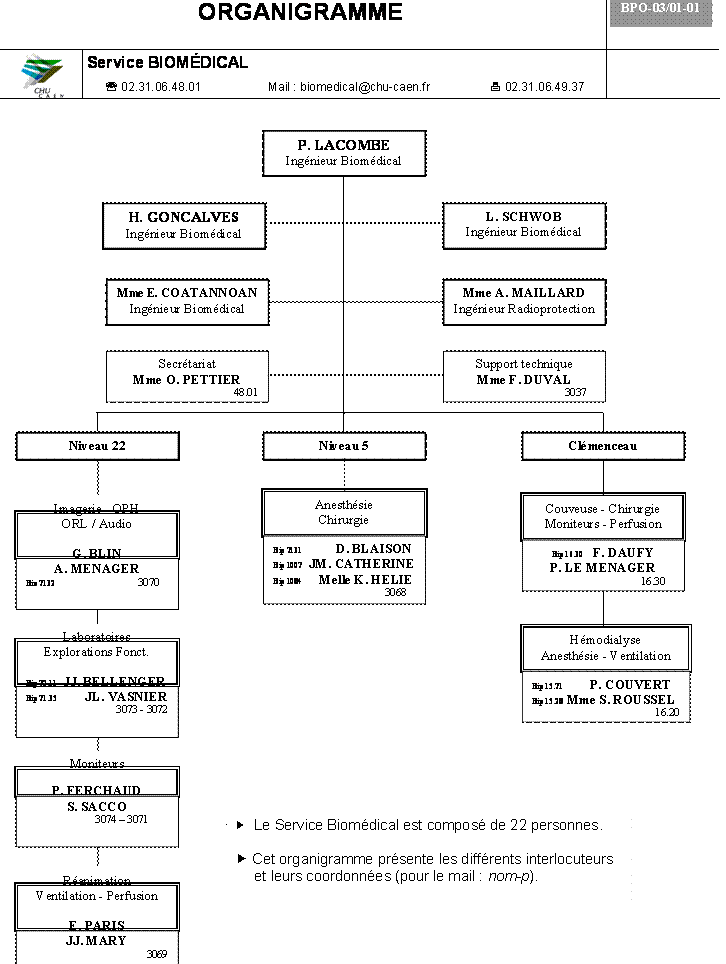
figure 13 : Organigramme
du service biomédical [24]
1.6
Fonctionnement du
service
biomedical
1.6.1
Role du service
biomedical
Le
service biomédical a pour rôle la prise en charge et le
suivi des équipements. Leurs missions évoluent autour des
principaux axes suivants [6]
-
la maintenance et le contrôle
qualité des équipements et accessoires
-
l'acquisition des dispositifs
médicaux
-
la matériovigilance, la surveillance
des dispositifs médicaux
-
l'assistance des utilisateurs,
leur formation.
1.6.2
Patrimoine
biomedical
Un
patrimoine
biomédical ne peut être bien géré et
maîtrisé, que s'il est parfaitement connu, d’où
l’intérêt d’une GMAO à jour et correctement
renseignée.
1.6.2.1
Inventaire
L'inventaire
est l'élément clé de la connaissance du parc des
équipements médicaux Il est basé sur une
nomenclature, des fichiers de données et un système
d'étiquetage.
La
nomenclature est nécessaire, c'est une obligation. Elle
représente la terminologie propre à une technique,
à une activité. C'est la base de toute méthode de
classement et d'identification standardisée, partagée et
surtout reconnue. Pour les équipements hospitaliers, la
nomenclature CNEH est utilisée par l'ensemble des
établissements depuis de très nombreuses années.
Celle-ci donne un code spécifique pour chaque domaine
d'activité et pour chaque type de matériel; par exemple :
Code
CNEH 32101
à
321 : Techniques opératoires
à 01 : Endoscopes
rigides.
retour
sommaire
Bien
souvent, les descriptions d'appareils sont affinées dans les
établissements pour être plus explicites et
détaillées. Au niveau de l'inventaire proprement dit, un
ensemble d'informations complète ces codes et descriptions et
renseigne ponctuellement chaque équipement.
On
trouve, par exemple :
-
sa fonction
-
son service et/ou centre de
charge
-
sa date de mise en service et
son prix
-
sa durée de garantie
-
sa configuration
-
son modèle et son
numéro de série
-
son fournisseur et son
constructeur
-
les personnes ressources,
responsables de la maintenance
La
totalité de ces données constitue la fiche de
l'équipement et lui confère son caractère unique.
Celui-ci est identifié par un numéro d'inventaire propre,
porté sur une étiquette. Celle-ci indique
également la localisation du matériel pour qu'il soit
facilement repéré par tous.
Pour
certains dispositifs, tels que les accessoires, l'instrumentation
chirurgicale ou les endoscopes, il est impossible de coller une simple
étiquette. Dans ce cas, on fait référence au
numéro de série du dispositif. Dans quelques
établissements, le gravage ou des systèmes plus
sophistiqués de code à barres sont adoptés.
1.6.2.2
Evolution
du patrimoine
biomedical
Dans
tous les cas, pour assurer une réelle maîtrise du parc,
permanente et à long terme, une saisie rigoureuse et des
corrections permanentes sont nécessaires. Et ce, d'autant que de
nombreux acteurs alimentent la base de données ainsi
constituée.
D'autre
part, il est important de pouvoir adapter la structure de cet
inventaire pour l'évolution de son organisation, mais aussi des
techniques et des risques encourus.
Au
CHU de CAEN, le service Biomédical gère près de
12000 équipements . Chaque règle de saisie, chaque
évolution de la base de données est formalisée,
diffusée et connue de l'ensemble des personnes du service. Les
solutions d'échanges et de partage de l'information telles que
la messagerie ou les serveurs de données sont un atout
incontestable. Elles sont mises à profit pour valoriser chaque
action, chaque étape du processus que l'on peut intituler
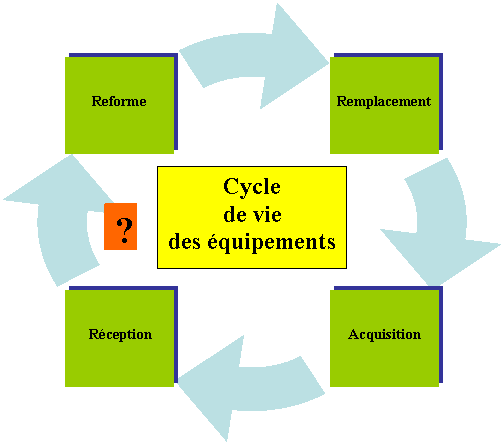
«Le cycle de vie des équipements».
1.6.3
Cycle
de vie des equipements
1.6.3.1
De l
acquisition a la reforme
Un
patrimoine se construit dès l'expression du besoin par les
services hospitaliers.
Les
projets d'acquisition ou d'équipements pluriannuels constituent
la programmation des investissements et permettent à ce titre :
-
de prévoir
l'évolution du patrimoine et des techniques
-
d'anticiper le renouvellement
des équipements
-
de maintenir le niveau des
performances, tout en favorisant l'innovation
On aborde également
à ce niveau la notion d'obsolescence - technologie
obsolète ou dépassée, ne répondant plus
à l'état de l'art ou aux besoins. L'état du
matériel doit donc être connu pour donner un avis
technique préalable à toutes décisions de retrait
ou de renouvellement.
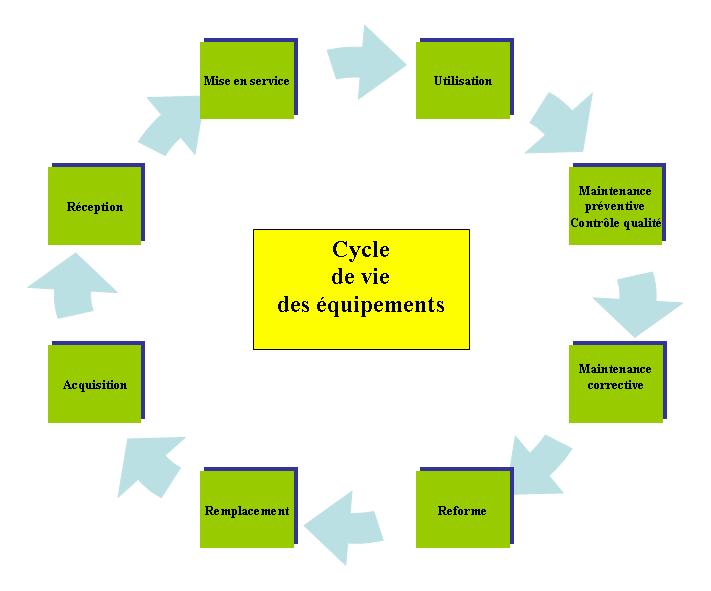
Figure14 :
Schéma du cycle de vie des équipements
gérés par le service biomédical [25]
1.6.3.2
Tracabilite
La
GMAO se construit autour de l'inventaire des équipements et
gère l'ensemble des activités liées de près
ou de loin à leur maintenance et aux ressources liées
à leur exploitation.
Ces
logiciels ont pu évoluer pour prendre en charge la gestion des
incidents propres à la matériovigilance, par exemple.
Le
CHU de CAEN a adopté cet outil et l'avons adapté à
la programmation des achats. Les équipements sont ainsi suivis
avant même qu'ils ne soient achetés. Il s’agit seulement
de lui créer un numéro d’inventaire provisoire !
Lorsqu'un
achat est envisagé, un ensemble de données est recueilli,
auprès du fournisseur. Il s'agit d'obtenir ou de prendre
connaissance des éléments suivants :
- le marquage CE
- le manuel d'utilisation
- la liste des accessoires ou consommables
- les modes de nettoyage, de désinfection
ou de stérilisation
- les recommandations techniques et la
documentation pour la maintenance.
Une fois
acquis, l'équipement intègre son parc après les
étapes de réception, de mise en service et de formation
des personnels utilisateurs et techniques.
Par
la suite, pour enrichir la base de données et alimenter
l'historique, la traçabilité des opérations de
maintenance, des incidents et des coûts, ce qui permettra au
responsable des équipements biomédicaux de
connaître plus précisément la composition et
l'état technique du parc.
Au
cours de la vie des équipements, ce mode de gestion du parc
permet de façon sélective de transmettre et d'assurer les
préconisations et obligations de l’AFSSAPS [7].
D’une réelle
connaissance du parc apporte une bonne réactivité dans la
conduite des alertes sanitaires, portant sur la sécurité
d'utilisation des dispositifs médicaux.
1.6.4
Fiabilite
des equipements
1.6.4.1
Entretien et
fiabilite
L'entretien
courant et la maintenance permettent de garantir ou de rétablir
les performances initiales des équipements, c'est-à-dire :
-
d'assurer la
sécurité des patients
-
de réduire la
vétusté
-
de répondre à la
réglementation et aux règles de l'art
Pour
les utilisateurs, il s'agit des phases de nettoyage,
désinfection, stérilisation, des changements de filtres
et accessoires, des contrôles de bon fonctionnement, de la bonne
association des équipements avec les dispositifs à usage
unique.
Pour
les techniciens, ce sont les actions correctives et
systématiques comme la maintenance préventive ou les
contrôles de qualité pour le maintien des performances.
Mais
aussi, et plus largement, des rappels d'usage et la formation sur le
terrain ou en écoles.
Grâce
au suivi permanent des interventions, la GMAO permet d'obtenir les
indicateurs sur :
-
la fiabilité des
équipements
-
les aspects techniques et
financiers
-
l'environnement utilisateur
C'est
également un outil indispensable pour :
-
la qualité du service en
termes de prestations
-
le partage et l'accès
à l'information
-
le développement de la
sécurité
Rappelons
qu'au sens de la norme X 60-010[8],
sur les concepts et définitions des activités de
maintenance, la sûreté de fonctionnement est
caractérisée par les quatre paramètres suivants :
-
fiabilité
-
maintenabilité
-
disponibilité
-
sécurité
1.6.4.2 Maintenance
systematique
Nous allons
à présent insister sur la notion de maintenance
systématique car elle est la base de toute politique d'assurance
qualité dans le domaine des équipements médicaux.
Trois
axes directeurs ont guidé notre démarche :
-
la gestion du patrimoine et des
risques
-
le développement des
actions préventives
-
l'accréditation
La
maintenance systématique a pour objectifs de :
-
limiter l'usure et
accroître la durée de vie
-
conserver les performances
initiales
-
réduire les pannes
techniques et les réparations
-
assurer les arrêts
programmés
-
augmenter la
sécurité d'utilisation
-
répondre aux
recommandations des constructeurs
-
respecter la
réglementation
Elle
s'inscrit dans un environnement général de
sécurité sanitaire. En effet, les actions
préventives et de contrôle portent en priorité sur
les équipements critiques ou sensibles, qui occupent une
position stratégique dans le processus de soin.
Pour
illustrer ces propos, le paragraphe suivant présente le cas
particulier de l'organisation mise en place au service
Biomédical du CHU de CAEN :
Dès
le projet d'acquisition d'un matériel, un dossier
d'équipement est constitué. Il est composé d'une
grille de questions, d'actions et d'étapes à effectuer
ainsi que d'une check-list permettant d'aborder les aspects à
considérer pour l'intégration d'un nouvel
équipement dans l'établissement. Cela va de la
documentation, aux contraintes d'installation, en passant par les
objectifs de maintenance ou les conditions de bon fonctionnement.
A
ce stade, les opérations systématiques de maintenance
préventive, de contrôle qualité, de calibration et
de vérification des performances, sont prévues. Elles
sont basées sur les recommandations des constructeurs, les
conditions d'utilisation, notre propre expérience et
l'appréciation des risques. Les contraintes économiques
sont à prendre en compte pour établir les
priorités.
Par
le biais de la base de données (GMAO), les objectifs de
maintenance sont fixés et inscrits pour chaque dispositif. Il
est important de pouvoir planifier et organiser ces actions et
d'informer les utilisateurs de leur réalisation.
Dans les
ateliers, des plannings couvrant 2 années permettent cette
planification et la répartition de la charge de travail; pour
l'ensemble des équipements dont les techniciens ont la charge.
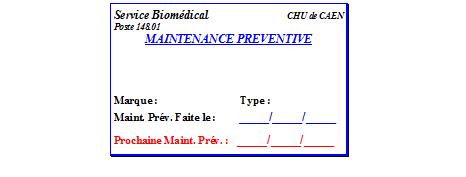
Après
chaque intervention, au niveau de chaque équipement, une
vignette est apposée selon le modèle suivant :
Figure
15 : étiquette de maintenance préventive [26]
Elle
fait apparaître le numéro d'inventaire du dispositif, sa
marque, son modèle, la date de la dernière maintenance
préventive et la date de la prochaine visite.
Ce
procédé permet de sensibiliser les utilisateurs sur les
obligations de contrôles et d'entretien des équipements,
tout en les informant des dates de maintenance.
La
mise en œuvre d'un ensemble d'outils et de méthodes n'est
pérenne que sur la base d'une organisation du travail
partagée et validée par l'ensemble des personnels du
service. A ce titre, des réunions régulières avec
les différentes équipes permettent d'établir les
objectifs et de passer en revue la charge de travail. Il s'agit
là de s'inscrire dans une démarche d'amélioration
continue propre à l'assurance qualité (roue de Deming) [9]. On parle aussi
d'évaluation, notion chère au processus
d'accréditation.
A
fréquence régulière, des bilans de situation sont
effectués, une analyse des écarts est
réalisée et les objectifs sont éventuellement
revus.
D'un
point de vue pratique, l'organisation mise en place a permis, en deux
ans, de doubler les actions de maintenance préventive sur le
parc de l'établissement, passant de 350 interventions
systématiques à plus de 700 par an en 2000 et 1360 en
2004.
2
Objectifs
2.1
Situation actuelle du materiel
de bloc operatoire suivi par le DPI
2.1.1
Limite de
fonctionnement
Le service
biomédical recense les besoins, réalise un plan
d’équipement, lance les appels d’offres, propose les essais,
achète le matériel.
Le
matériel est ensuite suivi par le DPI et est géré
différemment (base de données différentes entre le
service biomédical et le DPI).
Le dispositif
médical en fin de vie est réformé par le service
biomédical sur la demande du DPI.
Ce qui vient
à dire que le service biomédical n’a aucun suivi de la
vie des dispositifs médicaux gérés ainsi en ce qui
concerne les coûts, le nombre d’interventions et le temps que
chaque dispositif médical a engendré.
Figure16 :
Schéma du cycle de vie des équipements
gérés
mutuellement par le service biomédical
et
le DPI [27]
2.1.2
Relation
entre ces deux
services
retour
sommaire
Le responsable du service
biomédical a élaboré le guide de bonne pratique
qualité du CHU de CAEN, et a réalisé une
procédure claire concernant la relation entre le service
biomédical et le DPI.
Objectif :
Ce document définit les règles de fonctionnement entre le
service Biomédical et le Département Dépannage de
la DPI, pour les équipements médicaux et les
étapes suivantes :
1 -
Programmation
des
renouvellements
2 -
Acquisition
et
maintenance
3 -
Mise
en service et
réforme
1
Programmation
des renouvellements des équipements médicaux
La commission des achats médicaux
élabore chaque année un Programme d’Equipement
Médical soumis au Directeur Général.
Dans ce contexte, le service
Biomédical établit des recommandations dans le cadre
d’une politique de renouvellement des équipements
médicaux. Il sollicite au préalable le Département
Dépannage pour recueillir ses propositions argumentées en
matière de renouvellement.
|
-
Quand ?
|
La demande est
adressée à la DPI en juin.
Le
retour est attendu pour
la fin septembre.
|
|
-
Comment ?
|
Avec une grille de recensement précisant le motif du
renouvellement demandé et le numéro d’inventaire des
équipements.
|
retour
sommaire
2
Acquisition
et maintenance
Dans le cadre des procédures
d’acquisition, le Département Dépannage est
consulté par l’acheteur du service Biomédical pour
préciser ses attentes et recueillir ses avis.
|
-
Elaboration
du cahier des
charges
|
„
Définition
des
besoins et des prestations selon le type de matériel
(distinction entre base et option). Il est demandé aux
candidats de formuler des propositions pour :
-
des
contrats de
maintenance, du « préventif » au
«tous risques»…
-
la formation
des personnes
chargées de la maintenance de l'équipement.
„
Documentation
à
fournir, demandée au candidat :
-
le
programme des
opérations de maintenance systématique, de contrôle
et d’étalonnage indiquées par le fabricant (nature et
périodicité).
|
|
-
Au moment du choix
|
Pour initier la commande,
le service Biomédical adresse à la DSEE une Fiche
d’Accord et de Mise en service. Une copie accompagnée du devis
ou de l’offre correspondante est adressée au Département
Dépannage.
|
Mise
en service et Réforme
Pour
maîtriser l’inventaire du parc d’équipement, il est
important de gérer les entrées/sorties,
c’est-à-dire les phases de mise en service et de réforme.
|
-
Réception
|
La
réception des
équipements est assurée par le Département
Dépannage.
|
|
-
Mise en
service
|
Le
Département
Dépannage complète la Fiche d’Accord et de Mise
en Service et la retourne au service Biomédical. Le cas
échéant, cette fiche est complétée par le
procès-verbal de mise en service du fournisseur. Ces documents
sont ensuite adressés à la DSEE par le
Biomédical.
|
retour sommaire
2.1.3
Suivi inventaire
et base de donnees
Le DPI ne fonctionne pas avec une
GMAO comme le
service biomédical.
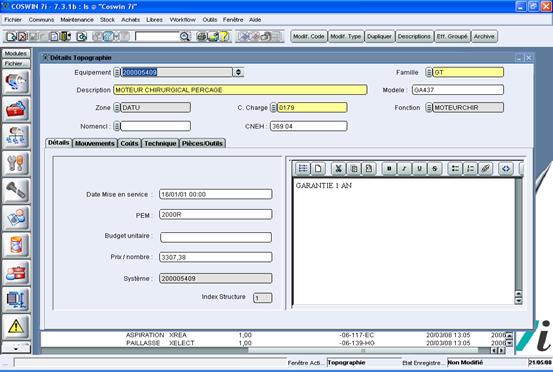
Le dispositif médical de par son acquisition par le service
biomédical est normalement inventorié sur la GMAO
qui est (COSWIN7i) [10]
avec son numéro d’inventaire son code CNEH etc.….
Figure
17 : détail topographie d'un équipement du
biomédical [28]
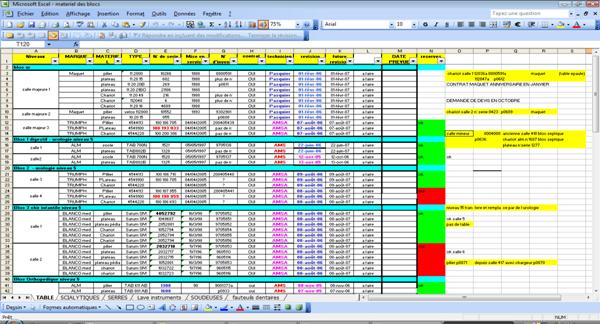
Le
DPI
fonctionne sur Excel avec le numéro de série et la
désignation du dispositif médical.
figure
18 : base de données de la DPI [29]
2.2
Moyen a mettre en
œuvre pour
avoir un suivi complet
2.2.1
Base
de donnees
biomedicale et du DPI
Le
premier
constat par rapport au fonctionnement entre le service
biomédical et le DPI est une base de données
différente.
Le
fait
d’avoir une base commune permettrait d’avoir un outil en commun sur la
gestion des dispositifs médicaux.
2.2.2
Connaitre
la vie du materiel
Le
dispositif
médical géré par le DPI n’a aucun suivi
informatique concernant la maintenance préventive, le
contrôle qualité et la maintenance corrective.
Aujourd’hui
l’ingénieur acheteur ne peut donner aucun chiffre sur le nombre
d’interventions de maintenance corrective, le nombre de pièces
détachées changées etc.….sur n’importe quel
dispositif médical géré ainsi.
2.2.3
La
maintenance et le controle qualite
Sur
les
équipements de bloc opératoire comme les tables et les
scialytiques, la maintenance préventive et le contrôle
qualité sont réalisés en externe.
La
maintenance
corrective est réalisée par le DPI sans aucune
procédure de contrôle qualité qui devrait
être réalisé après tout type d’intervention
comme par exemple le contrôle de sécurité
électrique après le démontage d’une table
opératoire ou le contrôle de luminosité
après le remplacement de lampe de scialytique.
Ces
interventions ne sont pas réalisés car les techniciens
n’ont pas de procédures et ne connaissent pas l’importance du
contrôle qualité sur les dispositifs médicaux.
Tout
ceci ayant
pour but d’assurer en toutes circonstances la sécurité
des patients mais aussi celle du personnel et des utilisateurs. Les
dispositifs médicaux doivent être conçus,
utilisés et entretenus avec le souci constant d’assurer un
très haut niveau de qualité.
2.2.4
Budget
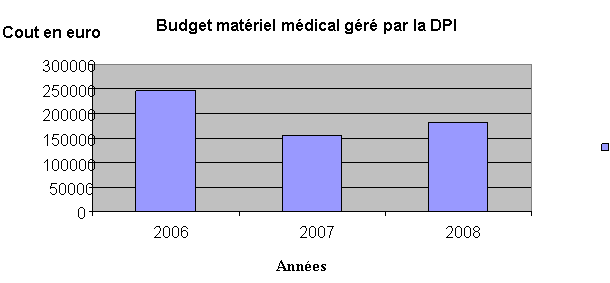
Je
me suis mis
en relation avec le magasin technique afin d’évaluer les budgets
concernant les dispositifs médicaux gérés par le
DPI.
figure 19 : budget matériel
médical géré par la DPI [30]
Toutes
ces
dépenses correspondent aux envois en réparation et
dépannage de tout genre et intègre quelques contrats de
maintenance.
Un
constat
important est qu’il y a très peu de contrat de maintenance. Un
exemple aucun contrat concernant la réparation des moteurs
chirurgicaux qui engendrent des sommes colossales (une consultation
pour cet exemple est peut être à prévoir pour
créer un contrat de maintenance).
2.2.5
Temps
necessaire
Concernant
le nombre de techniciens que cela nécessite, à ce jour
deux techniciens du DPI sont attitrés à la maintenance
dans les blocs opératoires, mais leurs activités ne sont
pas limitées aux dispositifs médicaux, ils s’occupent
également de la petite maintenance (ampoules, changement de
filtres de climatisations etc.…..).
3
Methode
3.1
Recherche sur les bases de
donnees
3.1.1
GMAO
biomedical
Le
logiciel de
GMAO COSWIN7i de part sa conception permet de réaliser des
filtres sur différentes rubriques, c’est à dire avec la
description du dispositif médical en tapant table par exemple
cela donne la liste de toute les tables répertoriées sur
la GMAO et ainsi de suite pour chaque rubrique, ce qui m’a permis
d’avoir la liste du matériel inscrit sur la GMAO pour chaque
bloc opératoire en ce qui concerne les tables, moteurs et
scialytiques.
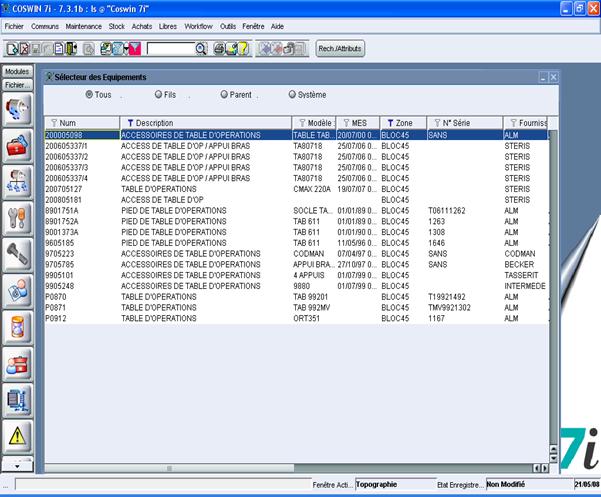
Figure
20 : copie
d'écran sur la sélection d'un équipement du
biomédical
[31]
retour
sommaire
3.1.2
Excel DPI
Excel
est
l’outil qui sert à la gestion du matériel médical
en inventoriant grâce aux numéros de série et
rarement avec le numéro d’inventaire biomédical. Ils ont
pour chaque bloc la liste de tables scialytiques et moteurs.
retour
sommaire
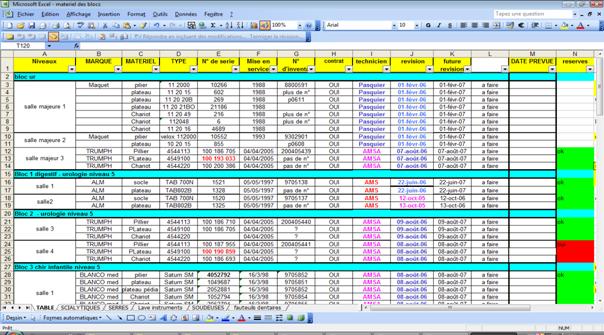
figure
21 : copie d'écran des tables opératoires de la DPI [32]
retour
sommaire
3.1.3
Inventaire contradictoire
et synthese
J’ai
réalisé pour chaque bloc opératoire avec les
données recueillies un comparatif entre les numéros de
série du biomédical et du DPI.
Le constat
à été très surprenant, pratiquement aucun
dispositif médical n’était commun aux deux services.
Le
résultat de la synthèse a été très
rapide, un inventaire terrain permettra une mise a jour aussi rapide.
3.2
Realisation de l inventaire
terrain
3.2.1
Methode pour table
et scialytique
L’inventaire
terrain concernant les tables, accessoires et scialytique a
été réalisé assez rapidement malgré
la problématique des blocs opératoires. Une amplitude de
travail de 10 heures avec des interventions programmées et des
urgences.
Donc la communication avec les surveillantes de blocs a
été indispensable afin d’avoir les informations pour
réaliser l’inventaire entre deux opérations.
Sachant
que le
CHU de CAEN dispose de 38 salles de bloc, ces opérations ont
demandé une organisation rigoureuse et se sont quand même
réalisées en quelques semaines
3.2.2
Methode
pour les moteurs
La
problématique se situe sur les moteurs. Les moteurs sont en
boite stérile, les chirurgiens les utilisent et ils sont mis au
lavage directement et envoyés en sachet à la
stérilisation. Donc un temps très court pour la
réalisation de l’inventaire.
J’ai
soulevé le problème avec mon responsable et les cadres
des différents blocs opératoires. L’inventaire sera
réalisé par les IBODES après utilisation.
Afin
de
faciliter la tâche des IBODES, j’ai réalisé une
liste des moteurs présumés avec leurs numéros de
série. Le premier retour était que les données du
service biomédical et du DPI étaient fausses.
Le
problème des moteurs est que, seul le numéro de
série permet de les identifier (pas de possibilité
d’installer des étiquettes à cause de la
stérilisation).
Le
parc
étant assez vieillissant, le nombre d’envois en
réparation assez important avec des chassés
croisés de moteur, avec ou sans échanges standard ce qui
sans avoir un suivi rigoureux sème la zizanie en un rien de
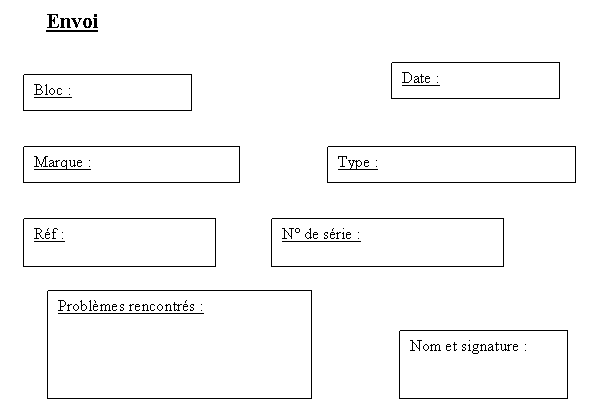
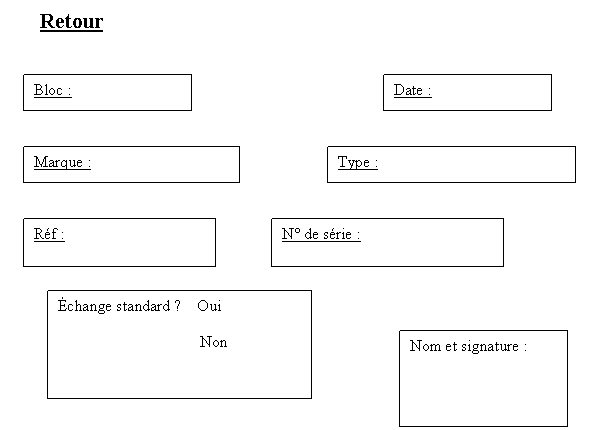
temps. C’est pour cela que j’ai proposé une fiche de suivi lors
d’un envoi de moteur avec deux parties (une partie envoi et une partie
retour) (annexe2), ce
qui permettra d’avoir une trace pour des remises à jour
régulière.
3.2.3
Synthese
Bilan
de cet
inventaire, il y a beaucoup de matériel avec une mauvaise
affectation, énormément de numéro de série
erronés. Concernant le recensement sur la GMAO, beaucoup de
matériel est présent mais pas répertorié et
également beaucoup de matériel est déclassé
sur la GMAO mais pas présent. Donc le manque de communication,
de base de données communes sont la cause de ce
dysfonctionnement.
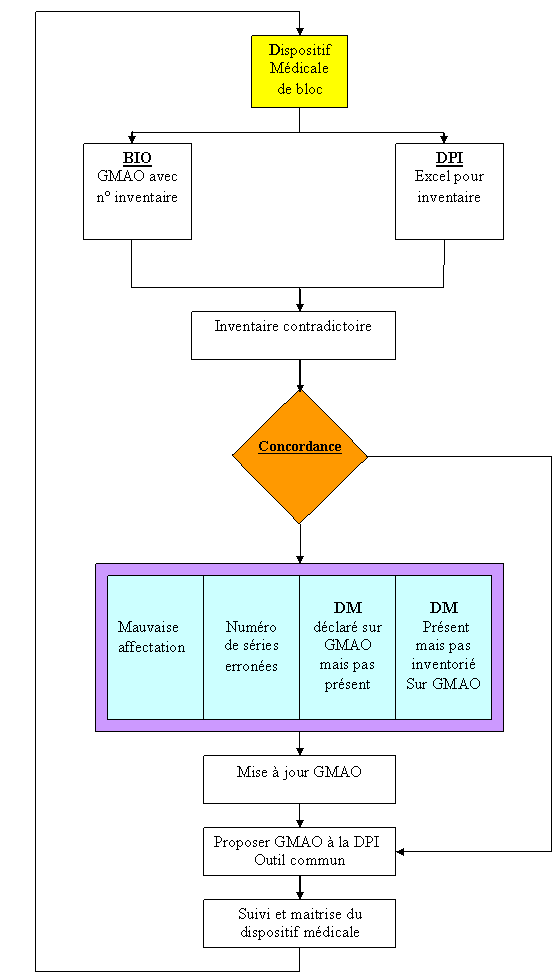
figure22:
méthode pour l'inventaire [33]
3.3
Installation de la GMAO au DPI
Suite au
constat réalisé sur le dysfonctionnement de l’interface
service biomédical, DPI, l’installation d’une GMAO au DPI est
incontournable.
Du
fait d’avoir un inventaire à jour, le DPI a tous
les éléments pour travailler sur la GMAO. Ce
qu’elle permettra est représenter ci-dessous.
figure 23 : diagramme d'Ishikawa
représentant la fonctionnalité d'une GMAO [34]
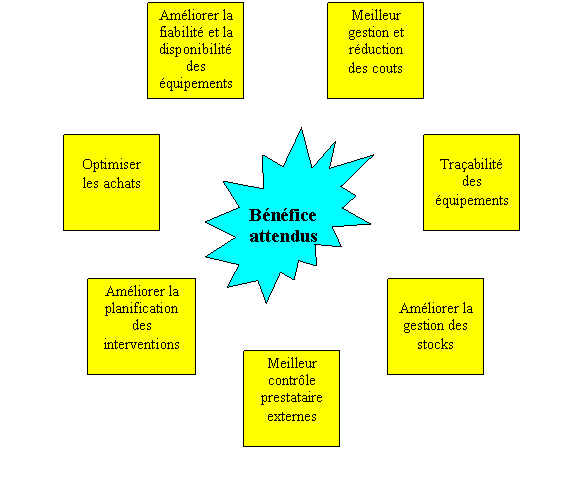
Les
bénéfices attendus de la gestion de la GMAO sont
représentes par ce diagramme :
figure24: Bénéfices
attendus lors d'une installationde GMAO [35]
Après
la
présentation de la GMAO au DPI, une période d’environ une
semaine de formation est indispensable pour avoir toutes les
compétences afin de pouvoir utiliser le logiciel assez
aisément et de comprendre l’intérêt d’une
traçabilité.
Afin
de pouvoir
évaluer le changement depuis l’installation de la GMAO, la
création d’une fiche d’auto-évaluation mensuelle (annexe3)
m’a
semblé indispensable afin de pouvoir mesurer ce changement et
permettra de connaître l’évolution du DPI et de cerner les
points à améliorer.
Des indicateurs de performance
pourront ensuite être utilisés(nombre de rapport
papier/nombre sur GMAO, coût en fournisseur papier/coût en
fournisseur GMAO) [11].
Figure 25 : Cycle PDCA appliqué
à la place de la GMAO à la DPI [36]
Moyen de
communication :
Le
manque de
communication a été un critère au manque de suivi
du matériel médical. Une fois la GMAO mise à jour,
les techniciens formés, la fiche d’auto évaluation
diffusée, il me semble important d’instaurer une réunion
mensuelle pour faire le point sur tous les problèmes
rencontrés, ce qui permettra une meilleure collaboration entre
les deux services qui ont un mode de fonctionnement différent et
qui se situe géographiquement à deux endroit
opposés de l'établissement.
Le service biomédical
se situe au 22 ème étage alors que le DPI se situe au
niveau 0.
3.4
Proposition de procedure du
controle qualite
Parallèlement
à cette démarche concernant le matériel
géré par le DPI, j’ai trouvé important de proposer
des procédures de contrôle qualité pour les
scialytiques et les tables opératoires car les techniciens
réalisent des interventions correctives sans réaliser de
contrôle qualité, ce qui permettra de les inciter à
réaliser ces contrôles et de les sensibiliser sur
l’importance de réaliser un contrôle qualité.
Ils
pourront par la suite imposer au prestataire extérieur de
remplir leur propre protocole de contrôle qualité pour
être en adéquation sur leur mode de fonctionnement. C’est
pour cela que je leur ai proposé pour ces deux
équipements cités ci-dessus un guide de contrôle
qualité rédigé par l’AAMB, ABIF, AFIB et la
SNITEM. (Annexe 4 et 5), afin de
développer la maintenance préventive et le contrôle
qualité.
retour
sommaire
3.5
Perspectives
Tout
ce travail
prévu afin de réorganiser la gestion du matériel
médical du DPI, permettra de connaître les coûts de
maintenance, le temps que cela nécessite par dispositif
médical, à condition que le DPI « joue le
jeu » et rentre toutes les interventions de maintenance,
tous les coûts de réparation, tous les coûts de
pièces détachées ainsi que le temps passé
à chaque intervention.
Cela,
dans
l’optique d’intégrer une équipe au service
biomédical capable d’avoir des éléments mesurables
pour déterminer le nombre de techniciens et le budget
nécessaires.
Cette
mise en
place permettra d’avoir les éléments nécessaires
et indispensables à la maîtrise du parc dans les
années à venir.
Elle aura
aussi pour intérêt de fournir des valeurs précises
quant aux données économiques, financières, et
horaires (équivalents temps plein) si le service
biomédical souhaite réintégrer dans son
fonctionnement la maintenance de ces équipements et avoir une
vision totale de son parc.
4
Conclusion
A
l’issue de
ces 11 semaines de stages effectuées au CHU de Caen, cette
nouvelle expérience dans le domaine biomédical m’a
été très enrichissante aussi bien du point de vue
relationnel que fonctionnel.
Tout
d’abord,
cela m’a permis de connaître un autre établissement, un
autre fonctionnement et une autre organisation de travail que
l’hôpital ou je travaille.
Ensuite,
les
différentes tâches qui m’ont été
attribuées m’ont permis de m’impliquer dans la fonction de
technicien biomédical (inventaire, travail sur organisation
GMAO, maintenance, contrôle qualité…..).
En
effet les
différents thèmes abordés m’ont permis de
travailler sur l’optimisation du matériel de bloc
opératoire géré mutuellement entre le service
biomédical et le DPI, mais aussi de réfléchir sur
les moyens d’aborder les problèmes et de rechercher des
solutions pour leur résolution.
Je
souhaite aux
services biomédical et au DPI que mon travail leurs aura donner
les outils nécessaires à la mise en place de la GMAO au
sein du DPI , et les aura sensibiliser sur la necessité de
developper des moyens de communications.
Et toujours
prendre en considération le but primordial : tout ceci a
pour but bien sur d’assurer le bon fonctionnement des dispositifs
médicaux et surtout de garantir la sécurité des
patients.
5
Glossaire
GMAO :
Gestion de la Maintenance Assistée par Ordinateur
CHU :
Centre Hospitalier Universitaire
DPI :
Département Patrimoine et Infrastructure
CNEH :
Centre National de l’Expertise Hospitalière
AFSSAPS :
Agence Française de Sécurité Sanitaire des
Produits de Santé
IBODE :
Infirmière de Bloc Opératoire Diplômé d’Etat
BPQ :
Bonne Pratique Qualité
AAMB :
Association des Agents de Maintenance Biomédical
SNITEM :
Syndicat National de l’Industrie des Technologie Médical
ABIF :
Association des Biomédicaux d’Ile de France
ATD :
Association des Techniciens de Dialyse
AFIB :
Association Française des Ingénieurs Biomédicaux
6
Bibliographie
Références
[1]
Décret
n°2001-1154 du 5 décembre 2001, http://www.utc.fr/~Farges/textes_off/lois/Decret_2001_1154.htm
[2]
Historique du CHU de
CAEN, http://www.chu-caen.fr/pagemodele.php?idpage=32
[3]
Sites du CHU de CAEN, http://www.chu-caen.fr/pagemodele.php?idpage=31
[4]
Répartition
des lits du CHU de CAEN,
http://www.chu-caen.fr/pagemodele.php?idpage=33
[5]
Les
équipements, http://www.chu-caen.fr/pagemodele.php?idpage=34
[6]
Bonne pratique
qualité du CHU de CAEN Mr LACOMBE Pierre
[7]
AFSSAPS, http://afssaps.sante.fr/
[8]
Normes X60-010,
http://www.utc.fr/tsibh/public/tsibh/05-06/projets/Normes%20essentielles/honore_pinard_taglia.html
[9]
La philosophie de Mr
DEMING cour de Mr Gilbert FARGES
[10]
GMAO COSWIM7i http://www.siveco.com/?lang=fr
[11]
Résolution
de problème cour de Mr Gilbert FARGES
Illustrations
[12]
Plan du CHU de CAEN
[13]
Fin des travaux
[14]
Bâtiment IRM
[15]
Projet
d’implantation de nouveau bâtiment
[16]
Hôpital Cote
de Nacre
[17]
Hôpital
Clémenceau
[18]
Centre de Personnes
Agées
[19]
Tableau de
répartition des lits
[20]
scanner du CHU de
CAEN
[21]Laboratoire
[22]
Salle de bloc
opératoire
[23]
répartitions
des dépenses du biomédical
[24]
Organigramme du
service biomédical du service biomédical du CHU de CAEN
d’après le BPQ
[25]
Schéma du
cycle de vie des équipements gérés par le service
biomédical réalisé par LAURENT
Frédéric
[26]
Etiquette de
maintenance préventive du CHU de CAEN d’après le BPQ
[27]
Schéma du
cycle de vie des équipements gérés
mutuellement
par le service
biomédical et le DPI réalisé par LAURENT
Frédéric
[28]
Détail
topographique d’un équipement du biomédical
d’après COSWIN7i
[29]
Base de données du DPI d’après document Excel
[30]
Tableau du budget
du matériel médical géré par le DPI
réalisé par LAURENT Frédéric
[31]
Copie
d’écran sur la sélection d’un équipement
biomédical d’après COSWIN7i
[32]
Copie
d’écran des tables opératoires du DPI d’après Excel
[33]
Méthode de
l’inventaire réalisé par LAURENT Frédéric
[34]
Diagramme
d’Ishikawa représentant la fonctionnalité d’une GMAO
d’après LAURENT Frédéric
[35]
Bénéfice attendus lors d’une installation d’une GMAO
d’après LAURENT Frédéric
[36] Cycle PDCA appliqué
à la place de la GMAO au DPI d’après LAURENT
Frédéric
7
Annexes
Annexe
1
Décret no 2001-1154 du 5
décembre 2001 relatif à
l'obligation de maintenance et au
contrôle de qualité des dispositifs médicaux
prévus à l'article L. 5212-1 du code de la
santé publique (troisième partie : Décrets)
NOR
: MESP0123968D
Le Premier
ministre,
- Sur le rapport
de la ministre de l'emploi et de la solidarité et du ministre
délégué à la santé,
- Vu la directive 97/43/EURATOM du Conseil
du 30 juin 1997 relative à la protection sanitaire des personnes
contre les dangers des rayonnements ionisants lors de l'exposition
à des fins médicales, remplaçant la directive
84/466/EURATOM ;
- Vu le code de la
santé publique, notamment ses articles L. 5212-1, L. 5212-2,
L. 5312-1, L. 6122-11, L. 6122-13, R. 665-7, R. 665-12 et R. 665-49,
Décrète
:
Art.
1er.
I. Il est inséré, à la section 1 du chapitre
Ier du livre V bis du code de la santé publique
(troisième partie : Décrets), les articles D. 665-5-1
à D. 665-5-4 ainsi rédigés :
«
Art. D. 665-5-1. - Pour l'application des dispositions du
présent livre :
« 1) On
entend par "exploitant" d'un dispositif médical toute
personne physique ou morale assurant la responsabilité juridique
de l'activité requérant l'utilisation de ce dispositif ;
« 2) On
entend par "maintenance" d'un dispositif médical
l'ensemble des activités destinées à maintenir ou
à rétablir un dispositif médical dans un
état ou dans des conditions données de
sûreté de fonctionnement pour accomplir une fonction
requise ; les conditions de réalisation de la maintenance sont
fixées contractuellement, s'il y a lieu, entre le fabricant ou
le fournisseur de tierce maintenance et l'exploitant ;
« 3) On
entend par "contrôle de qualité" d'un dispositif
médical l'ensemble des opérations destinées
à évaluer le maintien des performances
revendiquées par le fabricant ou, le cas échéant,
fixées par le directeur général de l'Agence
française de sécurité sanitaire des produits de
santé ; le contrôle de qualité est dit interne,
s'il est réalisé par l'exploitant ou sous sa
responsabilité par un prestataire ; il est dit externe, s'il est
réalisé par un organisme indépendant de
l'exploitant, du fabricant et de celui qui assure la maintenance du
dispositif.
«
Art. D. 665-5-2. - L'exploitant veille à la mise en œuvre de
la maintenance et des contrôles de qualité
prévus pour les dispositifs médicaux qu'il exploite. La
maintenance est réalisée soit par le fabricant ou sous sa
responsabilité, soit par un fournisseur de tierce maintenance,
soit par l'exploitant lui-même.
«
Art. D. 665-5-3. - En application de l'article L. 5212-1, le ministre
chargé de la santé après avis du directeur
général de l'Agence française de
sécurité sanitaire des produits de santé
arrête la liste des dispositifs médicaux soumis
à l'obligation de maintenance, celle des dispositifs
médicaux soumis au contrôle de qualité interne
et la liste des dispositifs médicaux soumis au
contrôle de qualité externe.
«
Art. D. 665-5-4. - Pour chacun des dispositifs soumis au contrôle
de qualité interne ou externe, le directeur
général de l'Agence française de
sécurité sanitaire des produits de santé
définit les modalités particulières de ce
contrôle, en fonction des dispositifs, par décision
publiée au Journal officiel de la République
française. Pour ce qui concerne les dispositifs médicaux
exposant les personnes à des rayonnements ionisants, les
décisions du directeur général de l'Agence
française de sécurité sanitaire des produits de
santé sont prises au vu de l'avis de l'organisme
désigné par l'autorité administrative
compétente en matière de radioprotection.
Le directeur général de l'Agence française de
sécurité sanitaire des produits de santé fixe
notamment :
«
- les critères d'acceptabilité auxquels doivent
répondre les performances ou les caractéristiques des
dispositifs médicaux soumis au contrôle de qualité
interne ou externe ;
« - la nature des opérations de contrôle
à mettre en œuvre pour s'assurer du maintien des performances
des dispositifs médicaux et les modalités de leur
réalisation ;
« - la périodicité des contrôles et
les situations nécessitant un contrôle en dehors des
contrôles périodiques ;
« - la nature des opérations de maintenance des
dispositifs médicaux qui nécessitent un nouveau
contrôle en dehors des contrôles périodiques ;
« - les recommandations en matière d'utilisation et de
remise en conformité compte tenu des dégradations ou
des insuffisances de performances ou des caractéristiques
constatées ainsi que, le cas échéant, les
délais laissés à l'exploitant pour remettre en
conformité les dispositifs. »
II. Il
est inséré, au chapitre Ier du livre V bis du code de la
santé publique (troisième partie : Décrets) une
section 10 ainsi rédigée :
«
Section 10 : Mise en œuvre de l'obligation de maintenance et du
contrôle de qualité
«
Art. D. 665-5-5. - Pour les dispositifs médicaux
mentionnés à l'article D. 665-5-3, l'exploitant est
tenu :
«
1o De disposer d'un inventaire des dispositifs qu'il exploite,
tenu régulièrement à jour, mentionnant pour chacun
d'eux les dénominations commune et commerciale du dispositif, le
nom de son fabricant et celui du fournisseur, le numéro de
série du dispositif, sa localisation et la date de sa
première mise en service ;
« 2o De définir et mettre en œuvre une organisation
destinée à s'assurer de l'exécution de la
maintenance et du contrôle de qualité interne ou externe
des dispositifs dont il précise les modalités, qui sont
transcrites dans un document ; dans les établissements de
santé, cette organisation est adoptée après avis
des instances médicales consultatives ; elle est portée
à la connaissance des utilisateurs ; les changements de cette
organisation donnent lieu, sans délai, à la mise à
jour du document ;
« 3o De disposer d'informations permettant
d'apprécier les dispositions adoptées pour l'organisation
de la maintenance et du contrôle de qualité interne ou
externe, ainsi que les modalités de leur exécution ;
« 4o De mettre en œuvre les contrôles prévus
par l'article D. 665-5-4 ;
« 5o De tenir à jour, pour chaque dispositif
médical, un registre dans lequel sont consignées
toutes les opérations de maintenance et de contrôle de
qualité interne ou externe, avec pour chacune d'elles
l'identité de la personne qui les a réalisées et,
le cas échéant, de son employeur, la date de
réalisation des opérations effectuées et, le cas
échéant, la date d'arrêt et de reprise
d'exploitation en cas de non-conformité, la nature de ces
opérations, le niveau de performances obtenu, et le
résultat concernant la conformité du dispositif
médical ; ce registre doit être conservé cinq ans
après la fin d'exploitation du dispositif,
sauf dispositions particulières fixées par
décision du directeur général de l'Agence
française de sécurité sanitaire des produits de
santé pour certaines catégories de dispositifs ;
« 6o De permettre l'accès aux dispositifs
médicaux et aux informations prévues par le
présent article à toute personne en charge des
opérations de maintenance et de contrôle de qualité.
«
Art. D. 665-5-6. - Le contrôle de qualité externe des
dispositifs médicaux est réalisé par des organismes
agréés à cet effet par décision du
directeur général de l'Agence française de
sécurité sanitaire des produits de santé
publiée au Journal officiel de la République
française. L'agrément précise les tâches
pour lesquelles il est accordé.
«
L'agrément est accordé pour une durée de cinq
ans renouvelable, en fonction des garanties d'indépendance
et de compétence présentées, de
l'expérience acquise dans le domaine considéré et
des moyens dont l'organisme dispose pour exécuter les
tâches pour lesquelles il est agréé. La composition
du dossier de demande d'agrément est fixée par
arrêté du ministre chargé de la santé
après avis du directeur général de l'Agence
française de sécurité sanitaire des produits de
santé.
« Les organismes qui satisfont aux normes les concernant,
transposant les normes européennes harmonisées, dont les
références ont été publiées au
Journal officiel de la République française, sont
présumés répondre à ces critères.
« Les organismes doivent s'engager à permettre aux
personnes désignées par le directeur
général de l'Agence française de
sécurité sanitaire des produits de santé
d'accéder à leurs locaux et de procéder à
toute investigation, afin de vérifier qu'ils continuent de
satisfaire aux conditions de l'agrément.
« Les organismes s'engagent en outre à communiquer au
directeur général de l'Agence française de
sécurité sanitaire des produits de santé toute
modification des conditions d'exercice de leurs activités,
telles qu'elles sont énoncées dans leur demande
d'agrément.
« Si un organisme agréé cesse de remplir les
conditions qui ont permis son agrément, celui-ci peut être
retiré par décision du directeur général de
l'Agence française de sécurité sanitaire des
produits de santé après que le responsable de l'organisme
a été mis à même de présenter ses
observations.
« Les organismes agréés établissent un
rapport annuel d'activité qu'ils communiquent au directeur
général de l'Agence française de
sécurité sanitaire des produits de santé. Ce
rapport d'activité mentionne, d'une part, la part du chiffre
d'affaires relative aux contrôles effectués dans le cadre
de cet agrément et, d'autre part, pour chacun des
contrôles de qualité effectués, le nom de
l'exploitant, le dispositif contrôlé, la nature des
contrôles réalisés et les non-conformités
observées.
« Art. D. 665-5-7. -
Les organismes agréés mettent en œuvre, à la
demande de l'exploitant, les contrôles conformément aux
dispositions particulières prévues à l'article D.
665-5-4.
« Chaque contrôle de qualité externe donne lieu
à l'établissement d'un rapport relatif au maintien
des performances du dispositif contrôlé. Ce rapport
mentionne le nom de l'exploitant, le dispositif contrôlé,
la nature des contrôles effectués et les
non-conformités observées. Il est remis à
l'exploitant qui en consigne un exemplaire dans le registre
mentionné au 5o de l'article D. 665-5-5.
« Art. D. 665-5-8. -
Dans le cas où un contrôle de qualité met en
évidence une dégradation des performances ou des
caractéristiques du dispositif, l'exploitant prend des
mesures appropriées relatives à l'utilisation et
procède à la remise en conformité du dispositif
conformément aux dispositions prévues à l'article
D. 665-5-4.
« Si les dégradations des performances constatées
sont susceptibles d'entraîner un risque d'incident tel que
prévu à l'article L. 5212-2, celui-ci fait l'objet d'un signalement
en application du même article , accompagné du rapport
mentionné à l'article D. 665-5-7, si le dispositif a fait
l'objet d'un contrôle de qualité externe.
« Art. D. 665-5-9. - Dans le cas du contrôle de
qualité externe, la remise en conformité des dispositifs
est attestée par les résultats conformes d'un second
contrôle de qualité réalisé sur le
dispositif selon les dispositions prévues à l'article D.
665-5-7.
« Si, après ce second contrôle, les performances
attendues du dispositif ne sont toujours pas atteintes, l'organisme
agréé informe le directeur général de
l'Agence française de sécurité sanitaire des
produits de santé.
« Art. D. 665-5-10. - Dans le cas où le contrôle de
qualité a conduit au signalement d'un risque d'incident
prévu par l'article D. 665-5-8, l'exploitant notifie au
directeur général de l'Agence française de
sécurité sanitaire des produits de santé la remise
en conformité du dispositif médical ou sa mise hors
service définitive.
« En cas de remise en conformité, si le dispositif
médical a fait l'objet d'un contrôle de qualité
externe, l'exploitant communique à l'Agence française de
sécurité sanitaire des produits de santé le rapport
mentionné à l'article D. 665-5-7 relatif au second
contrôle.
« Art. D. 665-5-11. - Quand le directeur général de
l'Agence française de sécurité sanitaire des
produits de santé a connaissance qu'un exploitant d'un
dispositif médical soumis au contrôle de qualité
n'a pas mis en œuvre les dispositions prévues par le
présent code, il met en demeure l'exploitant de faire
procéder à ce contrôle.
« Art. D. 665-5-12. - En cas de non-conformité d'un
dispositif médical, constatée à la suite d'un
contrôle de qualité, le directeur général de
l'Agence française de sécurité sanitaire des
produits de santé informe le préfet de
région, le directeur de la caisse régionale d'assurance
maladie, et, le cas échéant, le directeur de l'agence
régionale d'hospitalisation. »
Art. 2. - La ministre de l'emploi et de la solidarité et le
ministre délégué à la santé sont
chargés, chacun en ce qui le concerne, de l'exécution du
présent décret, qui sera publié au Journal
officiel de la République française.
Fait à Paris, le 5 décembre 2001.
Par le Premier
ministre : Lionel Jospin
La ministre de l'emploi et de la solidarité, Elisabeth Guigou
Le ministre délégué à la santé,
Bernard Kouchner
retour
sommaire